
Les dessins ci-dessous rťalisťs par un ťlŤve essaient d'expliquer le phťnomŤne.

1 Expťriences avec le gaz roux
 |
Quand on comprime, la coloration
du gaz devient plus foncťe. Pourquoi peut-on comprimer un gaz et pourquoi cette
coloration qui s'accentue? Les dessins ci-dessous rťalisťs par un ťlŤve essaient d'expliquer le phťnomŤne. |
|
| Le ballon infťrieur contient un gaz roux et celui du haut de l'air.Au bout de quinze minutes les colorations sont les mÍmes . Voici un schťma explicatif proposť par un ťlŤve. |
|
|
|
|
2 ModŤle du gaz
La nature ťtant complexe on imagine une image simplifiťe de la rťalitť. Cette image simplifiťe constitue un modŤle. Ce modŤle de la matiŤre sera affinť pour expliquer davantage de phťnomŤnes en quatriŤme puis en troisiŤme.
 |
Un gaz est formť de particules trŤs espacťes qui se dťplacent trŤs vite. Elles subissent des
millions de chocs par seconde entre-elles et contre les parois.
Pour voir une animation dans laquelle on peut modifier la tempťrature en dťplaÁant un curseur : http://www.andorra.ad/lycee_comte_de_foix/cinetique/cinetique.htm |
3 ModŤle du liquide.
| Un liquide est dense
et quasiment incompressible car les particules sont trŤs proches Les particules bougent en roulant les une sur les autres donc le liquide remplit tous les recoins du rťcipient. |
 |
4 ModŤle du solide
| Ce cube est un cristal naturel, il n'a pas ťtť taillť. On explique sa forme rťguliŤre par un empilement rťgulier de particules immobiles, comme si elle ťtaient collťes, donc le solide conserve sa forme. Un solide est lourd, et il est difficile ŗ comprimer car les particules sont serrťes. |
|
5 Simulation de la fusion d'un solide avec des billes.
| On filme des billes. Au dťpart elles sont bien rangťes comme dans un solide, puis elles se dťplacent ce qui reprťsente la fusion du solide. | 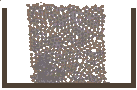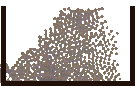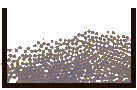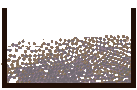 |
6 Taille des particules d'huile d'olive.
Les particules sont trŤs petites mais on peut calculer l'ordre de grandeur de sa longueur.
| Utiliser une cuvette bien propre et bien rincťe. On saupoudre la surface d'une cuvette ou d'un plateau de grande taille contenant de l'eau avec une poudre fine comme du talc ou de la poudre de carbone. |
| On prťlŤve une goutte d'huile d'olive. Son volume par comparaison ŗ un cube de 1mm3 de cŰtť est estimťe ŗ 0,3 mm3. Placťe sur l'eau elle s'ťtale en une couche ťpaisse d'une molťcule qui repousse la poudre noire. |
Le diamŤtre lu sur la rŤgle est d'environ 20cm=200 mm Donc le rayon vaut 100 mm.
Le volume de l'huile est le mÍme une fois ťtalť. La tache est un cylindre trŤs peu ťpais et e ťtant l'ťpaisseur :
V= 3,14 x R x R x e =
3,14 x 100 x 100 x e= 31400 x e et V = 0,3mm3 = 31400 x e donc e = 0,3/31400 = 0,000009 mm| mm | micromŤtre | nanomŤtre | ||||
| 0, | 0 | 0 | 0 | 0 | 0 | 9 |
Le rťsultat n'est pas prťcis mais il donne une idťe de la taille d'une molťcule que l'on ne voit pas.