à 0°C. C'est même ainsi que le physicien Celsius a défini le zéro de son échelle de température.
1 La fusion de la glace
 |
Si l'on fait fondre de la glace on constate que
la température se stabilise à 0°C. C'est même ainsi que le physicien Celsius a défini le zéro de son échelle de température. |
2 La solidification de l'eau.
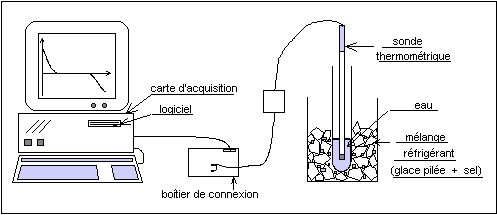
Le mélange réfrigérant glace + sel permet d'abaisser la température en dessous de zéro degrés.
Si vous voulez savoir comment on faisait des sorbets dans les châteaux de la renaissance, alors que le réfrigérateur n'a été inventé qu'au XIXème siècle. Cliquez sur SORBET
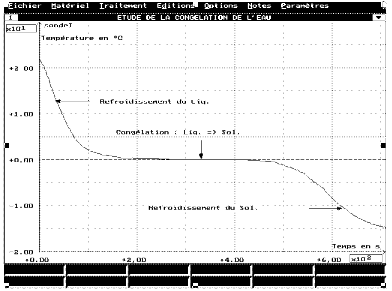
On constate qu'il existe un palier de solidification à 0°C. La température reste fixe tant que le tube contient de l'eau solide et de l'eau liquide. Ceci est une caractéristique de l'eau pure.
3 Conservation de la masse.
| Lorsqu'un glaçon fond la masse ne change pas. La masse se conserve. |
4 Variation du volume.
| Si l'on place un tube de verre plein d'eau bien fermée dans un congélateur il éclate car le volume de la glace est plus grand que celui de l'eau liquide. |   |
| Les glaçons en fondant diminuent de volume et l'eau ne déborde pas du récipient. |  |
 |
| La glace est donc moins dense que l'eau liquide et elle flotte, ce comportement est rare, pour la plupart des corps le solide plus lourd coule. Le château d'Amboise au fond montre que ce n'est pas le pôle nord mais la Loire en 1938. |
photothèque. Archives municipales de Tours |
5 Ébullition de l'eau sous la pression atmosphérique
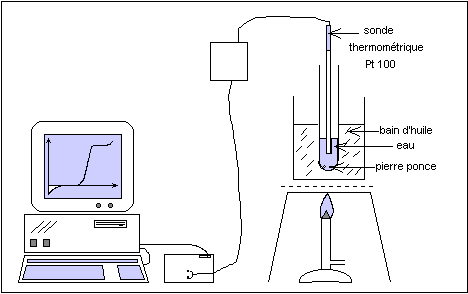
Le bain d'huile sert à chauffer régulièrement l'eau. L'huile ne bout pas car sa température d'ébullition est de 180°C.
Pour faire passer l'eau de l'état de liquide à celui de gaz il faut fournir de la chaleur, le passage inverse absorbe de la chaleur. Application la drôle de voiture à cascade d'eau.
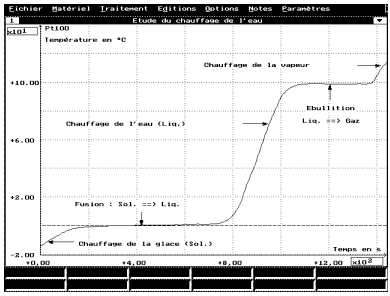
On constate qu'il existe un palier d'ébullition à 100°C. La température reste fixe tant que le tube contient de l'eau liquide et de l'eau sous forme de gaz. Ceci est une caractéristique de l'eau pure.
la même expérience décrite par l'abbé Nollet en 1748.
6 Ébullition sous une pression
différente 
6.1 La pression est plus faible que la pression atmosphérique
Si l'on diminue la pression au dessus de l'eau sa température d'ébullition diminue. Cela s'explique par le fait que les molécules d'eau sont moins "gênées pour décoller "et passer à l'état de gaz.
|
Avec une pompe on aspire l'air du ballon et l'eau bout à température ambiante. |
| La même expérience réalisée avec une seringue dans laquelle bout de l'eau à 20°C quand on tire sur le piston. |
|
6.1 La pression est plus grande que la pression atmosphérique
Le gaz situé au dessus de l'eau gène l'ébullition de l'eau qui ne s'effectue qu'à une température plus élevée. Dans un autocuiseur type "cocotte minute" l'eau bout à 105°C, 110°C la température étant plus élevée la cuisson est plus rapide.
| La pression est limitée par une
soupape qui se soulève dès que la pression dépasse une certaine valeur.
|
|
|
| Pour le cas où un aliment bouche la première soupape, pour éviter tout risque d'explosion une soupape de sécurité libère la vapeur. |  |
|
7 Variation du volume.
Quand l'eau bout le volume
occupé par la vapeur est beaucoup plus grand que celui de l'eau liquide. |
Il était illusoire de penser que la vapeur chasserait le boulet car la vaporisation devrait être instantannée pour être efficace. Le transfert de chaleur étant trop lent, ce canon ne vit jamais le jour. De plus il aurait fallu refroidir le canon pour un autre tir. |
| Léonard de Vincy proposa d'utiliser cela dans un canon à vapeur d'eau. Des charbons rouges sont versés dans le panier alors que de l'eau liquide se trouve coincé derrière le boulet. |
|
|
Photographies de la maquette exposée au clos Lucé à Amboise
Le principe des machines à vapeur
8 masse volumique de l'eau.
Un litre d'eau à 4°C possède une masse de 1 kg. On dit que la masse volumique de l'eau est de 1 kg/L. C'est une caractéristique de l'eau pure. La masse volumique de l'eau diminue quand on la chauffe car le volume augmente avec la température.
9 carte d'identité de l'eau.
